|
第一部分 采购邀请
为深入推进药品集中带量采购改革,根据《国务院办公厅关于推动药品集中带量采购工作常态化制度化开展的意见》(国办发〔2021〕2 号)等文件精神,由各省(区、市)及新疆生产建设兵团委派代表组成全国中成药联合采购办公室(以下简称联合采购办公室),代表上述地区相关医药机构开展全国中成药采购联盟相关药品集中带量采购。湖北省医疗保障局承担联合采购办公室日常工作并负责具体实施。
欢迎符合要求的企业前来申报。
一、采购品种及采购需求量
(一)采购品种清单
本次联盟地区集中带量采购品种及首年采购需求量(单位:万片/万粒/万袋/万支/万丸等),见表 1。
表 1 采购品种清单
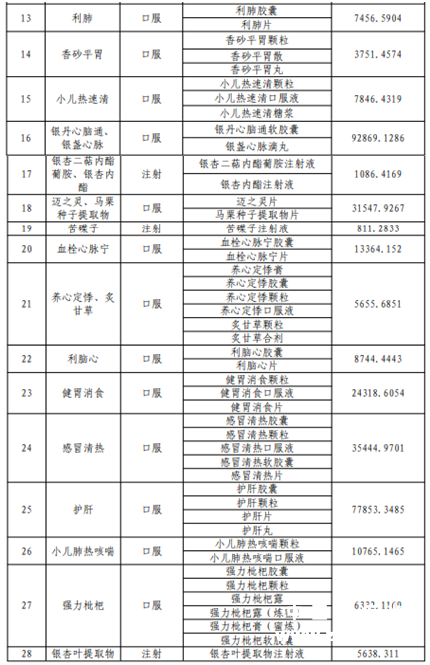
注:申报企业登陆“湖北医保服务平台”(https://ybj.hubei.gov.cn/hubeiHallSt/web/hallEnter/#/Index)查看采购数据。
(二)首年采购需求量
各采购组首年采购需求量按照参加本次集中带量采购的联盟地区医药机构实际填报的采购需求量累加确定。
二、采购周期与采购协议
(一)本次集中采购周期自中选结果实际执行之日起至2028 年 12 月 31 日。
(二)采购周期内采购协议可每年一签。续签采购协议时,联盟地区需综合考量医药机构上年度实际使用量、临床使用状况和医疗技术进步等因素,确定协议采购量,原则上不少于上年度协议采购量。采购协议也可签约至采购周期结束,同时在协议中明确每年采购量等相关内容。采购周期结束后,联合采购办公室综合考虑药品质量、供应稳定、信用优良、临床需求等因素开展接续工作。
(三)采购周期内若提前完成当年协议采购量,超出部分中选企业仍按中选价格进行供应,直至采购周期届满。 |